新闻动态
这种常见维生素竟能抑癌生长? 清华大学最新研究发布Cell子刊
2026-02-05

一盘三文鱼配菠菜,几颗开心果当零食,这些日常食物里藏着的维生素B6,可能正在为你的免疫系统打一场看不见的持久战。清华大学江鹏研究组最新发表在《发育细胞》期刊上的研究显示,这种普通得不能再普通的水溶性维生素,竟然能够让负责击杀癌细胞的T细胞保持干细胞样的年轻状态,延缓它们的疲劳和耗竭。更令人振奋的是,当维生素B6与免疫检查点抑制剂联用时,抗肿瘤效果提升到了一加一大于二的程度。
这项研究首次揭示了一个完整的分子机制链条:从食物中的维生素B6,到体内的活性形式磷酸吡哆醛,再到免疫细胞内部精密的信号调控,最终指向一个清晰的结论。营养素不仅是能量来源,更是免疫功能的深层调控者。
T细胞的耐力取决于代谢策略
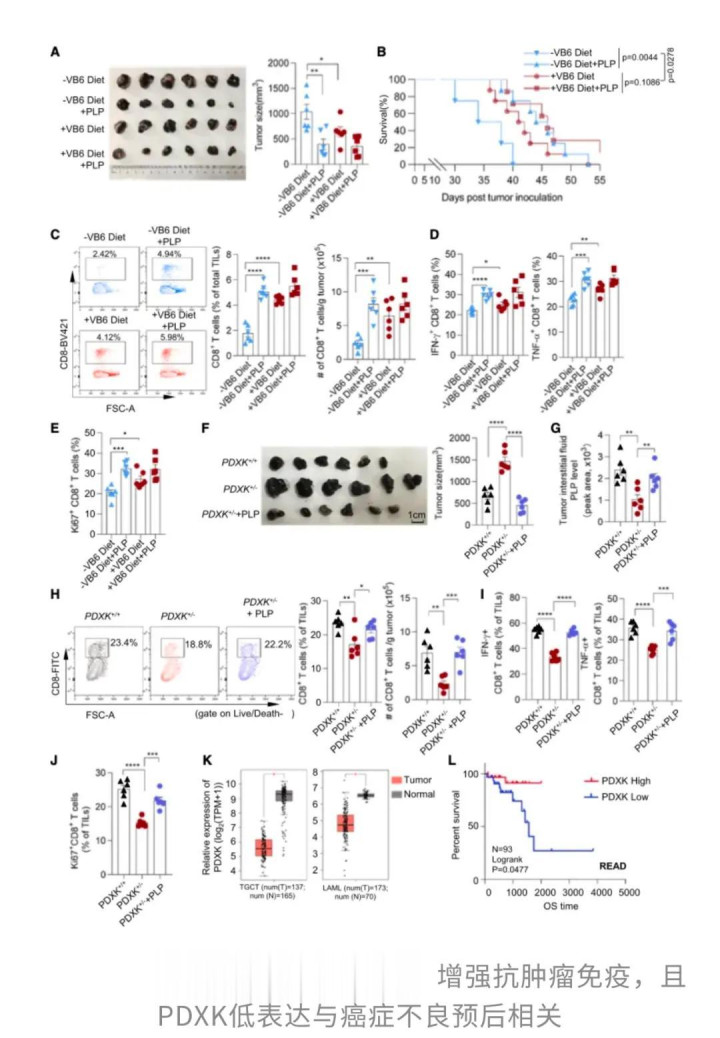
江鹏团队在黑色素瘤小鼠模型中进行的对照实验显示,缺乏维生素B6饮食的小鼠,肿瘤长得更快更大,而补充正常剂量维生素B6的小鼠,肿瘤体积明显缩小。最关键的差异出现在肿瘤浸润的CD8阳性T细胞上,这些被称为杀伤性T细胞的免疫战士,在维生素B6充足的环境中数量更多,分泌的干扰素伽马和肿瘤坏死因子等杀伤性分子浓度也更高。

但并非所有形式的维生素B6都有同等效果。在肺转移模型中,研究者发现只有补充其活性形式磷酸吡哆醛,才能显著减少转移灶数量,延长生存期。这种活性分子由一种名为吡哆醛激酶的酶负责生产,它就像维生素B6的加工厂,把原料转化成真正有战斗力的产品。
更有意思的是,这种补充即使在肿瘤形成之后进行,依然能够逆转局面。这意味着磷酸吡哆醛不仅可以预防,还能在癌症发展的中途介入,重新激活免疫系统。
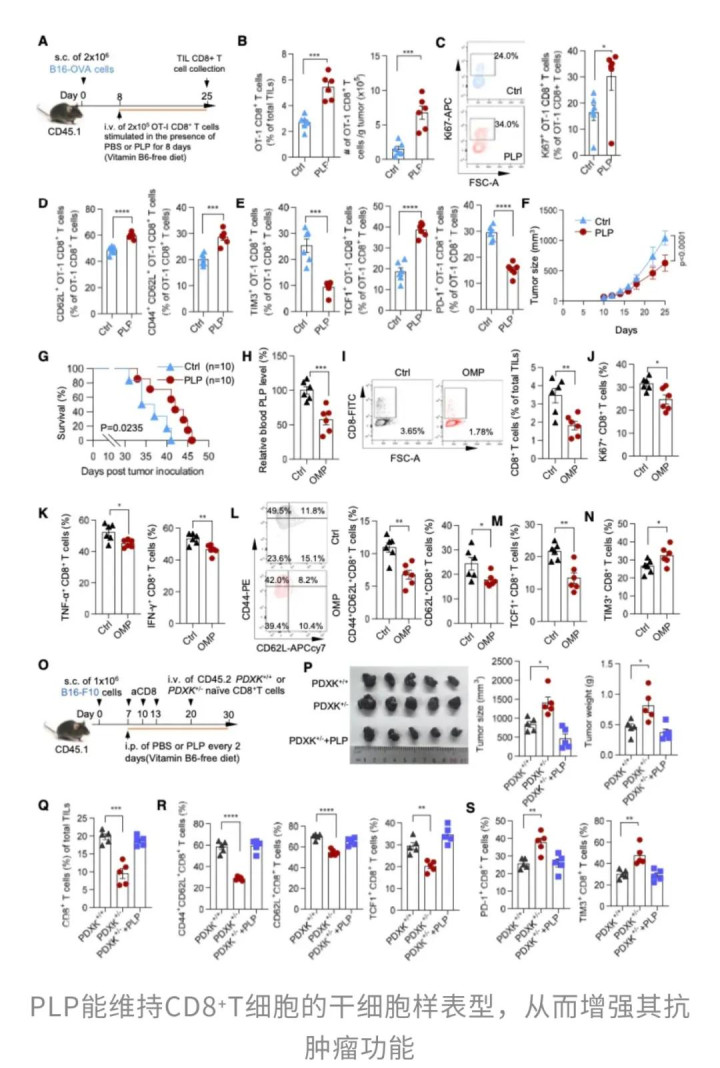
研究团队通过代谢组学分析发现,磷酸吡哆醛改变了T细胞的能量使用策略。正常情况下,效应T细胞偏好快速但不持久的糖酵解模式,这让它们像短跑运动员一样爆发力强但容易疲劳。而磷酸吡哆醛则推动T细胞转向线粒体氧化磷酸化这种更稳定的供能模式,让它们变成了马拉松选手,续航能力大幅提升。
分子层面的精准阻断
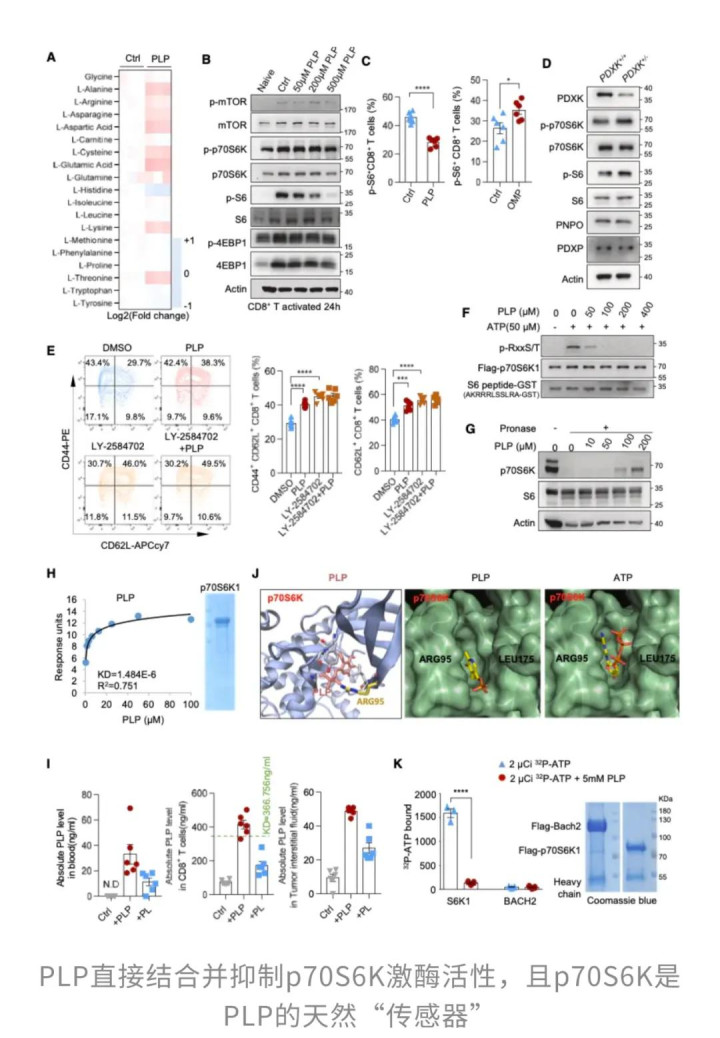
那么,这种代谢转换是如何实现的?答案藏在一个叫做p70S6K的激酶蛋白上。这个蛋白是细胞生长信号通路mTOR下游的关键节点,负责推动细胞进入高代谢、高增殖的工作状态。它通过给核糖体蛋白S6加上磷酸化标签,启动大规模的蛋白质合成。
磷酸吡哆醛的妙处在于,它能够直接抑制p70S6K的活性,让S6的磷酸化水平下降。一旦这条通路被踩了刹车,T细胞就不会被推向高消耗、易耗竭的轨道,而是保持在一种更具可塑性和持久性的状态。
更深层的机制涉及一个叫做BACH2的转录因子。这个蛋白通常待在细胞核内,负责激活维持T细胞干性的基因,同时抑制那些导致细胞耗竭的基因。但p70S6K会在BACH2的520位丝氨酸上打上磷酸化标签,把它赶出细胞核,导致干性基因失活。磷酸吡哆醛通过抑制p70S6K,让BACH2得以稳定留在核内,持续发挥作用。
这就好比给免疫细胞的指挥中心安装了一道防护锁,确保关键指令不会被错误关闭。
与免疫疗法的协同效应
清华团队还测试了磷酸吡哆醛与抗PD-1抗体的联合治疗效果。PD-1是T细胞表面的一个刹车蛋白,肿瘤细胞常常通过激活这个刹车来逃避免疫攻击。抗PD-1抗体的作用就是松开这个刹车,让T细胞重新活跃起来。
当磷酸吡哆醛与抗PD-1抗体联用时,抗肿瘤效果出现了明显的协同增强。单独使用磷酸吡哆醛或抗体都能在一定程度上抑制肿瘤生长,但两者结合后,肿瘤缩小得更快,小鼠存活时间更长,甚至有部分小鼠达到了完全缓解。
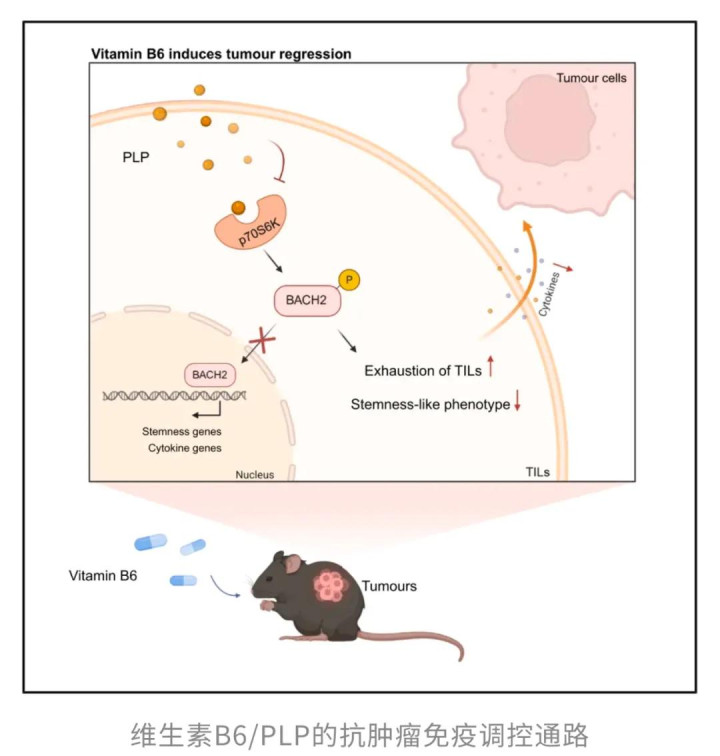
这个结果的意义在于,磷酸吡哆醛和免疫检查点抑制剂作用于不同的环节。前者从内部优化T细胞的质量和耐力,后者则从外部解除肿瘤施加的抑制。两者配合,等于既给战士升级了装备,又拆掉了敌人的防御工事。
从实验室到餐桌的距离
这项研究的临床转化前景值得期待。维生素B6是一种安全性极高的营养素,广泛存在于鸡肉、猪瘦肉、鱼类、全谷物、坚果和绿叶蔬菜中。对于正在接受免疫治疗的癌症患者,适当补充维生素B6可能成为一种简单而有效的辅助手段。
当然,从小鼠实验到人体应用还有很长的路要走。目前尚不清楚人类肿瘤患者需要多大剂量的维生素B6或磷酸吡哆醛才能达到最佳效果,也不清楚哪些癌症类型对这种干预最敏感。研究还发现,部分肿瘤如急性髓系白血病中吡哆醛激酶表达下降,这可能影响维生素B6的转化效率。
但无论如何,这项研究为我们打开了一扇新的窗口。它提醒我们,营养与免疫的关系远比想象中复杂而精密。那些看似平凡的食物分子,正在以我们尚未完全理解的方式,默默支撑着生命的防御系统。

